Острые инфекции верхних дыхательных путей множественной и неуточненной локализации (ОРВИ) остаются наиболее часто встречающимися заболеваниями у лиц любого возраста и составляют более 90% от числа всех инфекционных и паразитарных болезней в Российской Федерации [1]. Наибольшее число случаев заболеваний ОРВИ, как и в предыдущие годы, приходится на детей в возрасте до 17 лет (преимущественно периода раннего детства 1–2 года), их доля составляет 60–70% от всех зарегистрированных случаев респираторных вирусных инфекций [1]. Такая высокая распространенность ОРВИ среди детей во многом обусловлена как особенностями иммунной системы ребенка (незрелость, «поздний старт», отсутствие предшествующего иммунологического опыта), так и высокой контагиозностью респираторных вирусов.

Именно в периоде раннего развития ребенка отмечается наиболее высокий риск инфицирования, значительно чаще встречаются тяжелые формы ОРВИ с осложнениями [2]. Так, значительное место в структуре инфекционной патологии детей занимают пневмонии, причем, в первую очередь это касается новорожденных и детей первых месяцев жизни [3]. От пневмонии в мире ежегодно умирают от 750 тыс. до 1,2 млн новорожденных, что составляет 10% от глобальной детской смертности [4]. Этиология ОРВИ чрезвычайно разнообразна. Помимо гриппа выявлено более 200 вирусов, поражающих респираторный тракт.

При изучении пейзажа возбудителей ОРВИ среди госпитализированных детей, В.Н. Тимченко и др. установили лидирующую роль негриппозных патогенов (60,2%) с доминированием респираторно-синцитиальных вирусов (19,4%). Другие возбудители (парагрипп, адено-, рино-, метапневмо-, корона- и бокавирусы) в этиологической структуре ОРВИ встречались реже, однако в 10,7% случаев формировали микст-инфекции, в состав которых входило два (91,3%) и более (8,7%) вирусов [5]. Широкий спектр инфекционных агентов, число которых постоянно растет, и отсутствие средств специфической профилактики (кроме вакцин против гриппа) определяют сложности выбора эффективных и безопасных препаратов для предупреждения и лечения ОРВИ. Известно, что различная чувствительность респираторных вирусов, быстро развивающаяся резистентность затрудняют использование противовирусных средств, обладающих к тому же высокой токсичностью, в педиатрической практике. Риск суперинфицирования и активации условно патогенной микрофлоры обусловливает необходимость применения препаратов, обладающих одновременно этиотропным действием и иммуномодулирующей активностью, а также отсутствием каких-либо побочных эффектов [6]. Таким требованиям в полной мере отвечает препарат интерферона альфа-2b (ИФН-α2b) человеческого рекомбинантного с антиоксидантами ВИФЕРОН® Гель для наружного и местного применения [7].
Известно, что центральным звеном иммунной защиты от любых возбудителей ОРВИ является система интерферонов, которая осуществляет прямые и опосредованные противовирусные эффекты. У детей раннего возраста с инфекционно-воспалительными заболеваниями нарушается ее функционирование, что и лежит
в основе формирования заболеваний различных органов и систем [8]. Непосредственным виростатическим действием обладают ИФН I типа, приводящие через различные сигнальные пути к экспрессии ИФН-стимулированных генов, белковые продукты которых блокируют ключевые этапы жизненного цикла вируса, начиная с его внедрения в клетку и заканчивая высвобождением вирионов, при этом потенцируя адаптивные клеточные противовирусные реакции [9]. Кроме того, активизируя цитотоксическую активность Т-лимфоцитов, ИФН стимулируют лизис клеток, инфицированных вирусами [10].
На основании проведенного систематического поиска исследований, оценивающих клиническую эффективность и безопасность лекарственных средств, включая оценку уровня доказательности данных и методологию исследований, а также с учетом наличия в клинических рекомендациях и стандартах [11] нами проведено изучение влияния топической формы отечественного противовирусного препарата ВИФЕРОН® Гель на уровень заболеваемости ОРВИ в первые 3 месяца жизни в паре «мать – дитя» в условиях пандемии COVID-19.
Основной гипотезой, проверяемой в настоящем исследовании, явилось то, что интраназальное введение гелевой формы ИФН-α2b с антиоксидантами обладает профилактической эффективностью у новорожденных детей и их матерей в отношении ОРВИ. Кроме того, представлялось целесообразным сравнить результаты стандартной и произвольной (необязательной) схем применения хорошо изученного противовирусного препарата ВИФЕРОН® Гель, широко используемого при ОРВИ/гриппе.
Цель исследования: изучение профилактической эффективности интраназального применения препарата ВИФЕРОН® Гель для наружного и местного применения (интерферон альфа-2b) 36 000 МЕ/г в отношении ОРВИ
у новорожденных детей и их матерей в период пандемии COVID-19.
Пациенты и методы. В открытое проспективное сравнительное неинтервенционное наблюдательное исследование на базе МОНИИАГ первоначально было включено 300 пар матерей с новорожденными детьми. Все пациенты были ознакомлены с целями и задачами исследования и добровольно пожелали в нем участвовать. Критерием включения являлись новорожденные дети обоих полов и их матери, которые выписываются из родильного дома без дополнительных рекомендаций, а также наличие подписанного информированного согласия на участие в исследовании (единого для матери и ее ребенка). Критериями исключения в паре «мать – ребенок» служили подозрение на начальные проявления заболевания, имеющего сходную с ОРВИ симптоматику; необходимость применения медикаментозной терапии сопутствующих заболеваний, а также наличие терапии препаратами группы цитокинов и их индукторов или другими иммуномодулирующими препаратами в течение последнего месяца до начала исследования. Кроме того, отводом для включения в исследование матерей являлись такие анамнестические данные, как наличие ВИЧ-инфекции, сифилиса, гепатита B или C; алкогольной или наркотической зависимости; психических расстройств, требующих лечения антидепрессантами; участие в другом клиническом испытании в течение 3 месяцев до включения в настоящее исследование.
В результате проведенного отбора в марте – мае 2020 года в исследование были включены 227 пар «мать – новорожденный ребенок», соответствующих критериям включения и с отсутствием критериев исключения. Возраст женщин составлял от 20 до 50 лет, средний возраст – 33 ± 6,8 года, регион проживания – Московская область. Все дети родились с гестационным возрастом 37–41 недель, массой 2900–4100 г, ростом 48–54 см, оценкой по шкале Апгар на 1-й минуте – 7–8 баллов, на 5-й минуте жизни – 9 баллов у 95% новорожденных.
В зависимости от схемы профилактики включенные в исследование лица были разделены на три группы.
Первую группу (основную) составили 63 пары «мать – ребенок», получавшие препарат ИФН-α2b с антиоксидантами в лекарственной форме гель для наружного и местного применения 36 000 МЕ/г (ВИФЕРОН® Гель).
Препарат наносили на предварительно очищенную поверхность слизистой оболочки носа 2 раза в день в течение 4 недель в соответствии с инструкцией по медицинскому применению (полоска геля длиной не более 0,5 см). Во вторую группу (сравнения) вошли 50 пар «мать – ребенок», получавшие аналогичный препарат, но с нарушением схемы применения (прекратили использовать гель сразу после выписки, применяли нерегулярно или только при появлении симптомов заболевания).

Третью группу (контрольную) составили 114 пар «мать – ребенок», не получавшие профилактику. В случае появления заболевания проводили стандартную базисную терапию, рекомендуемую при ОРВИ. На каждую включенную в исследование пару «мать – ребенок» заполняли анкету, содержащую данные о матери (возраст, акушерский анамнез, роды, соматическая патология, условия проживания и др.) и новорожденном (возраст, рост, вес ребенка, вскармливание, аллергия/атопия и др.). Основными критериями для анализа эффективности профилактики являлись оценка частоты заболеваемости ОРВИ в паре «мать –дитя» в течение 3 месяцев после включения в исследование; определение длительности, выраженности течения каждого случая респираторных инфекций и клинических проявлений заболевания (лихорадка, интоксикация, катаральные симптомы); оценка частоты нежелательных явлений, связанных с применением исследуемого препарата. Статистическая обработка проведена с помощью пакета SPSS v23. Для количественных показателей определялся характер распределения (c помощью теста Шапиро – Уилка), среднее значение и стандартное отклонение, медиана, межквартильный интервал, минимальное и максимальное значения. Для категориальных и качественных признаков определялись доля и абсолютное количество значений. Сравнительный анализ для нормально распределенных количественных признаков проводился на основании t-теста Стьюдента (2 группы) или ANOVA (более 2 групп) с последующим попарным сравнением групп; для ненормально распределенных количественных признаков – с помощью U-критерия Манна – Уитни (2 группы) или критерия Краскела – Уоллиса (более 2 групп).
Сравнительный анализ категориальных и качественных признаков проведен с использованием критерия χ2 Пирсона, в случае его неприменимости – с помощью точного теста Фишера. Уровень значимости при проведении сравнительного и регрессионного анализа соответствует 0,05.
Результаты исследования и их обсуждение. В исследование были включены 227 пар «мать – новорожденный ребенок», соответствующих критериям включения и с отсутствием критериев исключения, которые в зависимости от проводимой профилактики были разделены на три группы: 1-я группа (n = 63) применяла препарат ВИФЕРОН® Гель в соответствии с инструкцией; 2-я группа (n = 50) применяла препарат ВИФЕРОН® Гель с нарушением рекомендуемой схемы, 3-я (контрольная) группа (n = 114) не получала профилактику (рис. 1).
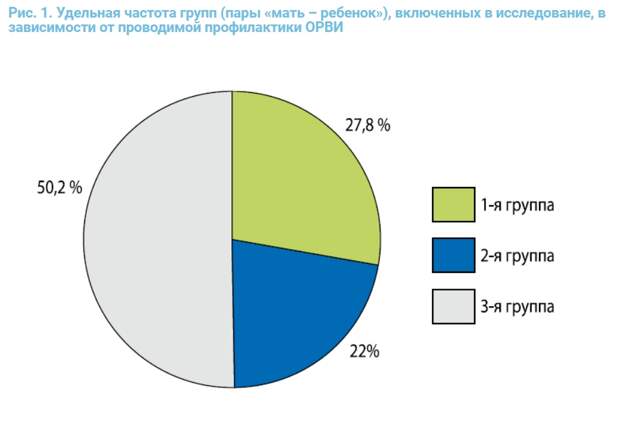
Возраст матерей на момент включения в исследование статистически значимо не различался в группах обследованных лиц, p = 0,694 (по критерию Стьюдента для независимых выборок с поправкой Уэлча на равенство дисперсий) (рис. 2).

Соматическая патология в виде заболеваний сердечно-сосудистой и нервной систем, почек, мочевыводящих путей и органов дыхания в стадии компенсации имела место у 45 (71,4%) матерей основной группы, 35 (70%) матерей группы сравнения и 80 (70,2%) матерей контрольной группы. У 125 (55,1%) женщин, включенных в исследование, роды были первыми, 102 (44,9%) женщины были повторнородящими. Через естественные родовые пути были родоразрешены 158 пациенток, частота операций кесарева сечения составила 30,4% и не имела статистически значимых различий в представленных группах. Антропометрические показатели, оценка по шкале Апгар, состояние здоровья в раннем неонатальном периоде не имели статистически значимых различий у новорожденных исследуемых групп. Все лица, включенные в исследование, были выписаны из родильного дома в марте – мае 2020 года с хорошим состоянием здоровья.
В процессе динамического наблюдения на протяжении последующих 3 месяцев во всех группах как у матерей, так и новорожденных детей были отмечены эпизоды ОРВИ, однако их частота варьировалась (табл. 1).
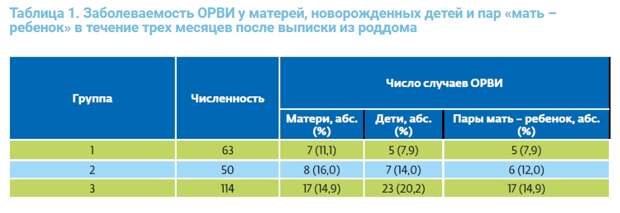
Проведенные наблюдения показали, что использование препарата ВИФЕРОН® Гель для профилактики ОРВИ способствует уменьшению числа эпизодов заболевания. Для подтверждения значимости этого утверждения был использован точный критерий Фишера, позволивший установить следующие статистические параметры. Частота
случаев ОРВИ у матерей в 1-й группе была меньше по сравнению с 2-й группой (11,1% против 16,0%) и 3-й группой (11,1% против 14,9%) (р = 0,578 и р = 0,647 соответственно), однако выявленная разница в уровне заболеваемости статистически недостоверна. Сходные результаты получены при сравнении показателей заболеваемости в группах 2 и 3 (16,0 и 14,9% соответственно; р = 0,818). Таким образом, матери, получавшие препарат ВИФЕРОН® Гель строго согласно инструкции, болели меньше, однако выявленная разница была незначима (табл. 1). У новорожденных детей, получавших препарат ВИФЕРОН® Гель, эпидемиологическая ситуация существенно отличалась.
Установлено, что заболеваемость ОРВИ у детей в группе 1 была достоверно меньше, чем в группе 3 (7,9% против 20,2%; тест Фишера р = 0,034). При сравнении групп 1 и 2 (7,9% против 14,0%; р = 0,363) не установлено столь значимых различий. В группе 2 заболеваемость детей ОРВИ также была меньше по сравнению с группой 3 (14,0% против 20,2%), но выявленная разница была незначима. Следовательно, при нерегулярном применении препарата и отсутствии его применения разница в заболеваемости ОРВИ практически отсутствовала в соответствии с точным тестом Фишера (р =0,389). Полученные данные свидетельствуют, с одной стороны, о выраженной профилактической эффективности препарата ВИФЕРОН® Гель, с другой – о необходимости соблюдения рекомендованной схемы применения препарата в соответствии с инструкцией. Сравнение заболеваемости ОРВИ между парами «мать – ребенок» показало, что они болели примерно одинаково в 1-й и 2-й группах, а между 2-й (нерегулярное или прекращение применения в профилактических целях препарата ВИФЕРОН® Гель) и 3-й группами (отсутствие профилактики) различий не было установлено (12,0% против 14,9%; р = 0,808) (рис. 3).
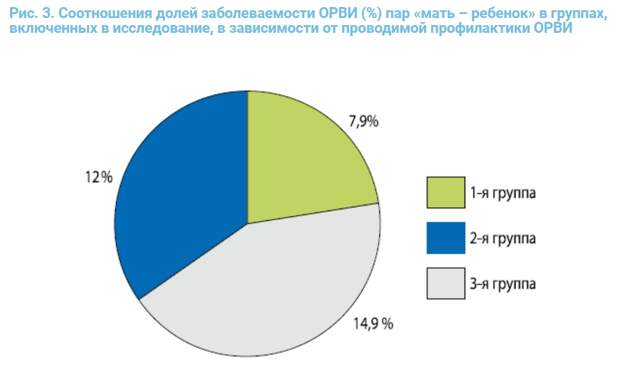
Таким образом, полученные данные свидетельствуют о достоверно значимом уменьшении эпизодов заболеваемости ОРВИ новорожденных детей, получавших профилактику препаратом ВИФЕРОН® Гель, по сравнению с контрольной группой. При анализе заболеваемости матерей и пар «мать – ребенок» в группе 1 отмечалась устойчивая тенденция к ее снижению. Эти результаты можно объяснить тем, что препарат ВИФЕРОН® Гель быстро усваивается в носо- и ротоглотке, обладает выраженным местным иммуномодулирующим действием и способствует увеличению локально образующихся антител класса секреторных IgA, препятствующих фиксации и размножению патогенных микроорганизмов на слизистых оболочках, что обеспечивает эффективность препарата [2]. Следует отметить, что все заболевания ОРВИ у матерей и детей основной группы были зарегистрированы на 3-м месяце после выписки из родильного стационара, причем в двух наблюдениях дети, имевшие контакт с больной матерью, не заболели. В контрольной группе и группе сравнения подавляющее большинство случаев заболевания ОРВИ (82,5 и 73,3% соответственно) были диагностированы в первый месяц после выписки. Эти результаты, с одной стороны, демонстрируют высокую профилактическую эффективность препарата ВИФЕРОН® Гель, а с другой – позволяют обосновать необходимость проведения повторных курсов профилактики при сохраняющемся высоком риске респираторных
заболеваний. Настоящее исследование было проведено в период пандемии новой коронавирусной инфекции COVID-19. По имеющимся данным, дети болеют с менее выраженной клинической симптоматикой, реже требуют
госпитализации, заболевание у них протекает легче [12]. Назначение ИФН-α2b с антиоксидантами для профилактики и лечения инфекции, вызванной SARS-CoV-2, у детей в нашей стране основывается в первую очередь на имеющихся данных об эффективности ИФН-α2b при лечении сезонных ОРВИ, в том числе и вызванных коронавирусами [5, 11,13]. В связи с этим в актуальных методических рекомендациях Министерства здравоохранения РФ отмечается, что для медикаментозной профилактики COVID-19 рекомендуется назначение интраназальных форм ИФН-α (у беременных возможно только применение рекомбинантного ИФН-α2b) [14, 15]. В нашем исследовании диагноз COVID-19 установлен у одного ребенка в группе нерегулярного приема препарата и у двух детей в контрольной группе. Во всех трех случаях заболевания протекали легко, с типичными симптомами ОРВИ, медианное значение продолжительности заболевания составило 4 (3,8–4,7) дня. Проведенные наблюдения показали, что использование препарата ИФН-α2b с антиоксидантами (ВИФЕРОН® Гель) с профилактической целью способствует сокращению длительности периода инфекционного процесса и ускорению выздоровления. Среднее число дней заболевания у детей в основной группе составило 2,8 ± 0,7, в то время как в группе сравнения и контроля – 5,3 ± 0,7 и 5,7 ± 1,1; значимость критерия Шапиро – Уилка – 0,031; 0,086 и 0,018 соответственно (табл. 2).
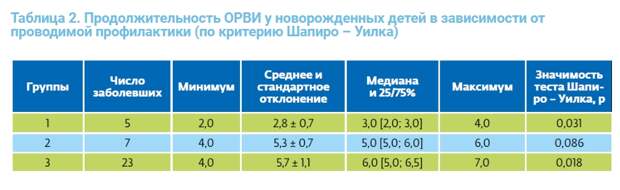
Исходя из попарного сравнения изучаемых показателей между группами по критерию U Манна – Уитни были получены статистически значимые различия в данных между 1-й и 3-й группами (р = 0,001), а также между 1-й и 2-й группами (р = 0,003), свидетельствующие о достоверном сокращении продолжительности течения респираторных инфекций в группе лиц, применявших ВИФЕРОН® Гель с целью профилактики в соответствии с инструкцией. Что касается сравнения длительности периода инфекционного процесса в группах 2 и 3, то значимые различия не установлены (р = 0,142). Динамика заболеваемости по сравниваемым группам представлена на рис. 4а. С учетом доверительных интервалов полученные результаты более наглядно могут быть визуализированы с помощью диаграмм с медианами, 25/75% и размахами (рис. 4).
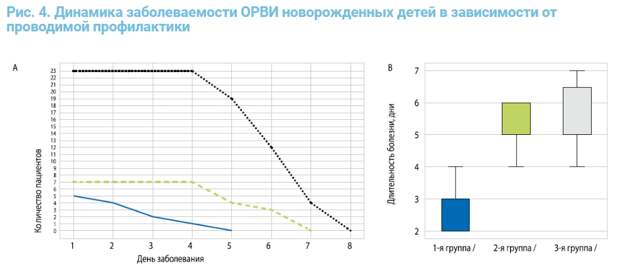
Анализ клинической симптоматики у больных детей, получавших с целью профилактики препарат ВИФЕРОН® Гель в соответствии с инструкцией, выявил его выраженный лечебный эффект, превысивший результаты, полученные в группах нерегулярного применения препарата и контроля. Минимальные и максимальные данные термометрии составили в 1-й группе 37,0 °С и 37,8 °С (37,6 °С и 37,8 °С (σ = 37,8 ± 0,2) и в 3-й –37,8 °С и 38,5 °С на у σ = 37,4 ± 0,3); в 2-й – (σ =37,9 ± 0,2) (табл. 3).
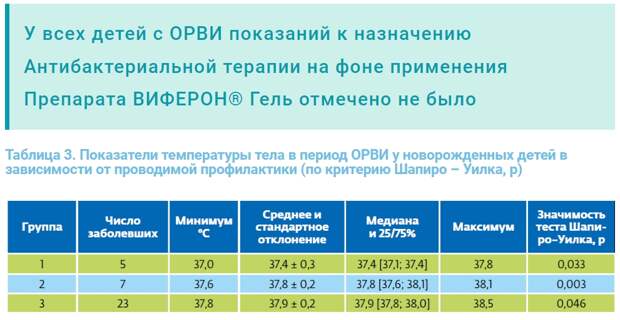
При попарном сравнении показателей температуры тела в период ОРВИ между группами по критерию U Манна – Уитни показано, что уровень гипертермии был значимо ниже в 1-й группе по сравнению с 2-й группой (р = 0,017) и особенно с 3-й группой (p = 0,015). В то же время между группами 2 и 3 выраженных различий установить не удалось (p = 0,278). Средняя продолжительность лихорадочного периода у детей в период заболевания ОРВИ в группе 1 была самой низкой и составила 3,2 ± 0,7 дня, в отличие от группы 2 (4,7 ± 0,9 дня) и группы 3 (4,4 ± 1,1 дня) (табл. 4).
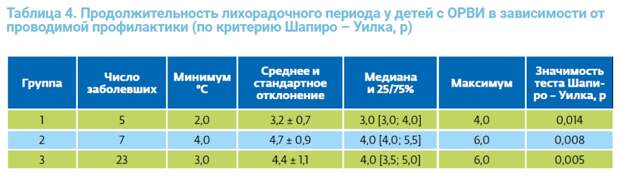
Анализ полученных результатов по критерию U Манна – Уитни показал, что продолжительность лихорадочного периода у детей с ОРВИ в группе 1 значимо короче, чем в группе 2 (p = 0,012) и группе 3 (p = 0,021), но между группой сравнения и контрольной группой разница не достоверна (p = 0,288). Таким образом, показатели температуры тела в период ОРВИ у новорожденных детей и продолжительность лихорадочного периода статистически достоверно меньше на фоне профилактического применения препарата ВИФЕРОН® Гель в соответствии с инструкцией, чем в группе нерегулярного использования препарата или среди детей в контрольной группе, не получавших профилактику. Примерно та же закономерность была обнаружена при оценке интенсивности и длительности катаральных симптомов ОРВИ. В отличие от пациентов групп 2 и 3, у детей, получивших профилактику препаратом ВИФЕРОН® Гель в соответствии с инструкцией, симптомы в виде кашля, ринита, снижения аппетита и симптомов интоксикации встречались реже и их продолжительность была значительно меньше. Во многом этому способствовал входящий в состав лекарственной формы препарата ВИФЕРОН® Гель антиоксидантный комплекс: α-токоферола ацетат, лимонная и бензойная кислоты, которые обладают противовоспалительным, мембраностабилизирующим, регенерирующим свойствами, а также обеспечивают сохранение биологической активности ИФН-α2b. Различия по средней продолжительности катаральных симптомов у детей в зависимости от проводимой профилактики оказались статистически значимыми (рис. 5).
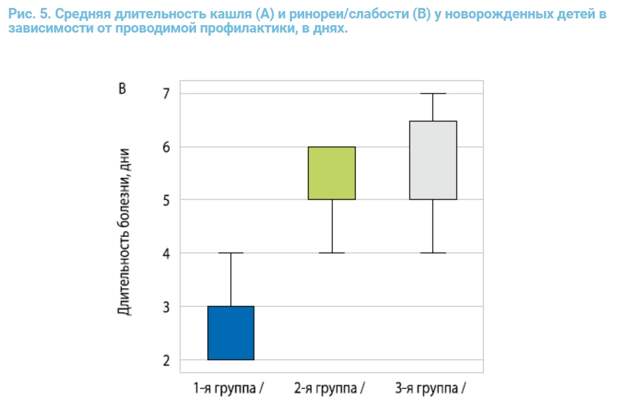
Так, средняя продолжительность кашля у пациентов группы 1 составила 3,3 ± 0,5 дня, а в группе 2 – 4,8 ± 0,7 дня (р = 0,032); продолжительность ринита и ухудшения самочувствия в виде слабости составила в группе 1 4,6 ± 0,5 дня, в группе 2 – 5,3 ± 0,5 дня (p = 0,033). Сравнение показателей между группами 2 и 3 (p = 0,174 и p = 0,092) не позволило выявить значимых различий, что еще раз подчеркивает тот факт, что нарушение схемы применения препарата ВИФЕРОН® Гель, его нерегулярное использование или прекращение применения после выписки из роддома приводят к отсутствию необходимого противовирусного и иммуномодулирующего действия. У всех детей с ОРВИ показаний к назначению антибактериальной терапии на фоне применения препарата ВИФЕРОН® Гель отмечено не было.
Препарат ВИФЕРОН® Гель хорошо сочетался с применяемыми симптоматическими средствами (жаропонижающими, сосудосуживающими, отхаркивающими). Оценка переносимости лекарственной формы ВИФЕРОН® Гель проводилась на основании мнения матерей 1-й и 2-й групп, которые в 100% случаев отметили хорошую переносимость препарата и удобство его нанесения на слизистую оболочку носовых ходов. Побочных действий препарата зарегистрировано не было, что позволяет сделать вывод не только об эффективности и целесообразности применения препарата ВИФЕРОН® Гель в паре «мать – ребенок» в первые месяцы после выписки из роддома, но и о безопасности применения препарата, в том числе у матерей в период лактации и у новорожденных, ввиду низкой абсорбции компонентов препарата. ВИФЕРОН® Гель с профилактической целью также целесообразно применять у детей, находящихся в непосредственном контакте с больными острыми респираторными заболеваниями.
ЗАКЛЮЧЕНИЕ
Полученные результаты исследования свидетельствуют о высокой профилактической эффективности, безопасности и хорошей переносимости препарата интерферона альфа-2b с антиоксидантами в лекарственной форме гель для наружного и местного применения (ВИФЕРОН® Гель), что позволяет рекомендовать его с профилактической целью новорожденным детям и их матерям в период высокой заболеваемости ОРВИ в условиях пандемии COVID-19. Отсутствие статистически значимых различий между группами пациентов, не применяющих препарат и применяющих его с нарушением схемы, диктует необходимость соблюдения инструкции к препарату для достижения максимального эффекта. Сроки манифестации заболеваний в группе пациентов, применяющих препарат в соответствии с инструкцией, позволяют обосновать необходимость проведения повторных курсов профилактики при сохраняющемся высоком риске респираторных заболеваний. Отсутствие случаев COVID-19 среди новорожденных, получавших профилактический курс препарата ВИФЕРОН® Гель на фоне пандемии, позволяет рекомендовать его применение в профилактике новой коронавирусной инфекции COVID-19 у новорожденных и подтверждает обоснованность его включения в клинические рекомендации по лечению COVID-19 у детей.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА
СПИСОК ЛИТЕРАТУРЫ
1. Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2019 году». – М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека. – 2020.
2. Шамшева О.В., Новосад Е.В., Полеско И.В., Учайкин В.Ф., Малиновская В.В., Семененко Т.А. /// Наружные формы рекомбинантного интерферона альфа-2b – мазь и гель в комплексной терапии ОРВИ и гриппа у детей. // Детские инфекции. – 2020. – 19 (2). – 42–46. DOI: 10.22627/2072-8107-2020-19-2-42-46
3. Романовская А.В., Давыдов А.И., Хворостухина Н.Ф. /// Особенности течения и исходы беременности при гриппе А/H1N1 swin. // Вопросы гинекологии, акушерства и перинатологии. – 2016. – 15 (5). – 26–31. DOI: 10.20953/1726-1678-2016-5-26-31
4. Заячникова Т.Е., Толокольникова Е.В., Красильникова А.С., Семененко Т.А., Шувалов A.Н., Малиновская В.В. /// Клинико-лабораторная эффективность человеческого рекомбинантного интерферона α-2b в составе комплексной терапии врожденной пневмонии у недоношенных детей. // Эпидемиология и инфекционные болезни. Актуальные вопросы. – 2019. – 9 (4). – 58–66. DOI: 10.18565/epidem.2019.9.4.58-66
5. Тимченко В.Н., Суховецкая В.Ф., Чернова Т.М., Баракина Е.В., Починяева Л.М., Малиновская В.В. и др. /// Роль ранней этиологической расшифровки острых респираторных вирусных инфекций в выборе противовирусной терапии у детей в условиях стационара. // Педиатрия им. Г.Н. Сперанского. – 2020. – 99 (1). – 15–22. DOI: 10.24110/0031-403X-2020-99-1-100-106
6. Кононова И.Н., Косовцова Н.В., Карева Е.Н., Поспелова Я.Ю. /// Интерферонотерапия в комплексе лечения вульвовагинитов у пациенток с многоплодной беременностью. // Вопросы гинекологии, акушерства и перинатологии. – 2019. – 18 (1). – 46–52. DOI: 10.20953/1726-1678-2019-1-46-52
7. Образцова Е.В., Головачева Е.Г., Осидак Л.В., Афанасьева О.И., Семененко Т.А., Выжлова Е.Н. и др. /// Рациональная терапия острых респираторных инфекций у детей раннего возраста препаратом рекомбинантного интерферона альфа-2b. // Инфекционные болезни. – 2020. – 18 (3). – 73–80. DOI: 10.20953/1729-9225-2020-3-73-80
8. Солдатова И.Г., Гетия Е.Г., Панкратьева Л.Л., Омельяновский В.В., Авксентьева М.В., Кущ А.А. и др. /// Оценка клинико-экономической эффективности препарата рекомбинантного интерферона α-2b человека – ВИФЕРОН® в комплексной терапии тяжелых неонатальных инфекций. // Педиатрия. Журнал имени Г.Н. Сперанского. – 2011. – 90 (5). – 67–76.
9. Калюжин О.В., Понежева Ж.Б., Купченко А.Н., Шувалов А.Н., Гусева Т.С., Паршина О.В. и др. /// Клиническая и интерферон-модулирующая эффективность комбинации ректальной и топической форм интерферона-α2b при острых респираторных инфекциях. // Терапевтический архив. – 2018. – 90 (11). – 48–54. DOI: 10.26442/terarkh201890114-54
10. Каграманова Ж.А., Ланщакова П.Е., Малиновская В.В., Свистунов А.А., Выжлова Е.Н., Жигалова Е.А. /// Факторы риска в
патогенезе неразвивающейся беременности по типу гибели эмбриона. // Вопросы гинекологии, акушерства и перинатологии. – 2020. – 19 (3). – 30–38. DOI: 10.20953/1726-1678-2020-3-30-38
11. Руженцова Т.А., Мешкова Н.А., Хавкина Д.А. /// Влияние терапии комбинированным препаратом интерферона альфа-2b с витаминами Е и С на течение ОРВИ и гриппа в детском возрасте: результаты мета-анализа. // Инфекционные болезни. – 2020. – 18 (2). – 68–79. DOI: 10.20953/1729-9225-2020-2-68-78
12. Методические рекомендации «Особенности клинических проявлений и лечения заболевания, вызванного новой коронавирусной инфекцией (COVID-19) у детей». Минздрав России. Версия 2 (03.07.2020).
13. Малиновская В.В., Семененко Т.А., Коржов И.В. /// Местные формы препарата интерферона альфа-2b с антиоксидантами в профилактике острых респираторных инфекций в организованных воинских коллективах в условиях пандемии
COVID-19. // Морская медицина. – 2020. – 6 (3). – 60–66. DOI: 10.22328/2413-5747-2020-6-3-60-66
14. Методическое пособие для врачей «Интерфероны: роль в патогенезе и место в терапии и профилактике COVID-19». Утверждено Учебно-методическим советом ФГБУ «Национальный медицинский исследовательский центр им. В.А. Алмазова» Минздрава России. 2020.
15. Временные методические рекомендации: профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Минздрав России. Версия 10 (08.02.2021).
Реклама
ОБЩЕСТВО С ОГРАНИЧЕННОЙ ОТВЕТСТВЕННОСТЬЮ "ФЕРОН"
ИНН 7704322416
125424, ГОРОД МОСКВА, ВОЛОКОЛАМСКОЕ ШОССЕ, ДОМ 73, ЭТ 6 П 1 К 46 ОФ 602, ОГРН: 1027739647220